Reaksi adisi aldehid
dan keton biasanya disebut dengan adisi nukleofilik. Reaksi adisi dapat
dikatakan adisi ketika dimana awalnya ikatan rangkap membentuk ikatan tunggal
atau tidak adanya ikatan rangkap. Aldehid dan keton memiliki sifat fisisnya
yaitu kepolaran dan kelarutannya. Coba perhatikan gambar dibawah ini:
Berdasarkan dari gambar diatas bahwa
aldehid dan keton memiliki atom C atau karbonil yaitu Sp2 , maka
sudut yang dibentuk ROH itu adalah 120o . Seperti yang kita ketahui
adalah bahwa keelektronegatifan O lebih besar dari pada keelektronegatifan C
sehingga itu menjadi ikatan yang polar.
Coba perhatikan perbandingan dibawah ini:
Dapat dilihat bahwa berdasarkan titik
didih yang paling rendah adalah alkana dan titik didih yang paling tinggi dari ketiga senyawa tersebut adalah
alkohol. Kenapa alkohol lebih tinggi titik didihnya dari pada yang lainnya?
Karena alkohol itu sendiri dengan alkohol yang lain dapat membentuk ikatan
hidrogen, sedangkan propanon dengan propanon lainnya tidak dapat membentuk
iktan hidrogen lainnya.
Selanjutnya berdasarkan
kelarutannya bahwa untuk senyawa alkanon yang mempunyai Mr rendah itu akan bisa
larut dalam air. Hal tersebut dikarenakan mempunyai ikatan hidrogen yang
terbentuk. Sehingga dapat disimpulkan bahwa aldehid dan keton merupakan senyawa
polar, karena bersifat polar maka reaksinya akan mudah bereaksi.
Lalu bagaimana, apa
perbedaan yang terjadi antara C=C yang merupakan bersifat non polar sedangkan
C=O merupakan senyawa karbonil yang bersifat polar?
Jika pada senyawa karbonil, dimana
diketahui bahwa O nya itu akan lebih elektronegatif sedangkan C akan lebih
elektropositif sehingga dengan demikian ketika adanya reaksi apabila sebuah
nukleofil yang bereaksi maka nukleofilnya akan menuju kearah C. namun sebaliknya
nanti ketika yang bereaksi itu adalah sebuah elektrofil yang kekurangan
elektron maka yang bereaksi dan melakukan penyerangan adalah atom oksigen.
Bagaiman reaksi aldehid dan keton pada umumnya? Coba perhatikan gambar dibawah
ini:
Bahwa reaksi aldehid dan keton diawali
dengan protonasi, dimana dapat dilihat atom O nya akan melakukan penyerangan
terhadap protonnya sehingga nanti akan terbentuknya reaksi. Kemudian akan
dilanjutkan dengan reaksi berikutnya dengan reaksi nukleofil, dimana
nukleofilnya akan melakukan penyerangan terhadap atom C sehingga atom C lebih
positif sehingga terbentuknya reaksi.
Dapat disimpulkan bahwa
umumnya karbonil itu selalu saja diawali dengan protonasi, setelah proton
diikat maka baru nukleofilnya akan melakukan penyerangan terhadap C nya
sehinnga nukleofilnya akan terikat. Dapat dilihat bahwa itu merupakan reaksi
adisi, hal tersebut dikarenakan yang awalnya ikatan rangkap kemudian berubah
menjadi ikatan tunggal.
Mekanisme
reaksi adisi nukleofilik sebagai berikut:
1.
Reaksi
Hidrat ( reakasi dengan air)
Dapat dilihat dari
gambar diatas bahwa gugus C=O harus di protonasi dengan H+ akan
menjadi OH dan muatannya menjadi positif.
Dapat dilihat bahwa elektronnya di C akan bergeser kearah O sehingga C
nya akan menjadi elektronpositif maka ketika elektron C nya positif dapat
diserang oleh nukleofil (H2O) yaitu O akan berikatan dengan C. Nah hasilnya adalah O nya akan bermuatan
positif sehingga akan melepaskan H+ akibatnya C akan mengikat OH dan
OH. Apa itu hidrat? Yaitu OH terikat pada C yang sama. Dapat dilihat bahwa
reaksi tersebut merupakan rekasi reversible, dimana reaksi reversible merupakan
reaksi yang kurang stabil.
2.
Reaksi
dengan alkohol ( hemiasetal dan asetal)
Pembentukan
reaksi dengan alkohol terbagi menjadi dua yaitu hemiasetal jika mengikat hanya
satu ROH saja sedangkan yang kedua yaitu asetal jika mengikat lebih dari sati
ROH ( mengikat 2 ROH). Dapat dilihat gambar dibawah ini:
Dapat dilihat bahwa selalu saja hal
pertama yaitu dilakukan protonasi, sehingga membentuk OH dimana O nya akan
bermuatan positif sehingga elektron C akan bergeser kea rah O menjadi C nya
lebih elektronpositif. Maka dengan C nya elektronpositif membuat nukleofilnya
dapat menyerang atom C. Maka akan terbentuknya OR dan O akan bermuatan positif
sehingga akan melepaskan H+ akibatnya akan menghasilkan senyawa
dimana C nya mengikat OH dan OR. Adapaun dari reaksi tersebut dapat disebut
sebagai hemiasetal karena itu untuk mengikat satu ROH. Bagaimana jika mengikat
dua ROH? Coba perhatikan gambar dibawah ini:
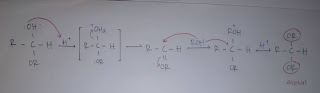
Adapun cara nya sama dengan langkah
sebelumnya yaitu adanya protonasi. Lalu manakah yang akan di protonasi OH atau
OR? Maka yang akan diprotonasi adalah OH. Hal tersebeut dikarenakan jika OR di
protonasi maka akan kembali seperti awal lagi makanya yang diprotonasi adalah
OH. Sehingga ketika OH nya diprotonasi maka akan terbentuk OH2 yang
bermuatan positif, dimana OH2 tersebut merupakan gugus yang mudah
pergi karena gugus pergi yang baik. Maka ketika OH nya lepas maka elektron dari
O itu akan bisa mengisi posisi dari C-R, C-O sehingga membentuk C=OR yaitu
membentuk ikatan rangkap. Dengan adanya ikatan rangkap tersebut maka C nya akan
terjadi pergeseran dimana ikatan rangkap O akan ke O. sehingga C nya akan
menjadi lebi positif dan ROH nya akan melakukan penyerangan terhadap C nya.
Adapun akibat dari penyerangan tersebut maka C nya akan mengikat ROH dan OR.
Selanjutnya H nya dilepas terbentuknya C yang mengikat OR dan OR. Jadi dapat
dilihat bahwa jika reaksi berlanjut maka akan menghasilkan reaksi asetal ( apabila
reaksi dilanjutnya dengan mereaksi ROH kembali maka akan menghasilkan reaksi
asetal).
3.
Reaksi
dengan Hidrogen sianida
Hidrogen sianida
merupakan asam lemah, biasanya reaksinya dalam suasa basa. Jika dalam suasa
basa akan menghasilkan H2O dan CN-. Dan CN-
ini lah yang akan bereaksi nantinya. Jika sebelumya kita sudah mengenal reaksi
H2O dan ROH, dimana kedua senyawa tersebut merupakan nukleofil lemah
maka jika nukleofilnya lemah membutuhkan protonasi sedangkan CN-
seperti yang diketahui bahwa merupakan nukleofil kuat sehingga tidak perlu
protonasi. Coba perharikan gambar dibawah ini:
CN- akan langsung melakukan
penyerangan terhadap gugus yang lebih posistig yaitu C, dengan demikian CN-
akan berpindah dan elektron dari akan bergeser membentuk O- . sedangkan
O- merupakan alkoksida yaitu basa yang kuat maka akan bereaksi dengan asam yang
lemah (HCN) sehingga kan mengikat H dan akibat yang terjadi C mengikat OH dan
CN (sianohidrid).
Permasalahan:
1. Reaksi
hidrat adalah reaksi reversible yang
merupakan reaksi yang kurang stabil. Jika reaksi hidrat tidak stabil, bagaimana
cara untuk menstabilkannya dan faktor apa saja yang dapat mensabilkannya?
2. Pada
reaksi dengan alkohol terdapat 2 yaitu hemiasetal dan asetal. Bagaiman kepolaran
yang terjadi ketika hemiasetal mengikat ROH yang membentuk karbonil mengikat OR dan OH sedangkan asetal mengikat 2 ROH yang mana karbonilya mengikat 2 OR?
3. Pada
reaksi dengan alkohol, dimana ketika OH diprotonasi pada reaksi asetal sehingga
terbentuknya OH2 atau H2O yang merupakan gugus pergi yang
baik. Bagaimana OH2 atau H2O dapat dikatakan gugus pergi
yang baik, padahal diketahui bahwa OH2 atau H2O merupakan
nukleofil lemah dan faktor apa yang menyebabkan OH2 atau H2O dapat
dikatakan gugus pergi yang baik?




















